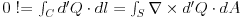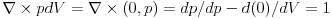Prvi zakon termodinamike u diferencijalnom obliku
d'Q=dU+d'W
d'Q,d'W-neegzaktni diferencijali - predstavljaju "male kolicine".
dU-egzaktan (neko kaze i totalni) diferencijal
Uzmimo primer sirenja gasa pri p=const.
d'Q=dU+pdV
d'Q=d(U+pV)
A H=U+pV je entalpija koja je fja stanja te je dH egzaktan diferencijal.
Pa imamo da je d'Q=dH tj. neegzaktan diferencijal je jednak egzaktnom diferencijalu?
Kako ovo objasniti?




 Egzaktni i neegzaktni diferencijali u fizici
Egzaktni i neegzaktni diferencijali u fizici